Оглавление
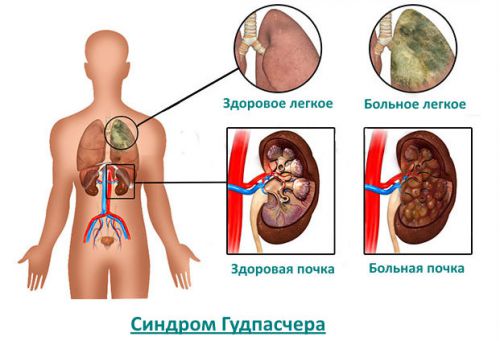
Синдром Гудпасчера – что это за патология

Синдром гудпасчера – это название стало именем нарицательным по фамилии Эрнеста Гудпасчера американского врача и патофизиолога. Именно он впервые в 1919 году описал случай легочного кровотечения и гломерулонефрита во время эпидемии гриппа.
На сегодняшний день этот термин используется для описания клинической сущности диффузного легочного кровотечения и острого или быстропрогрессирующего гломерулонефрита. Но исторически сложилось так, что именно проявление последнего ассоциирует с синдромом гудпасчера, хотя клиницисты определяют его как идиопатический быстропрогрессирующий гломерулонефрит. Характерный признак- наличие циркулирующих в крови антител к клубочковым базальным мембранам (анти – БМК), поэтому можно встретить еще и название «болезнь анти-БМК».
Как развивается
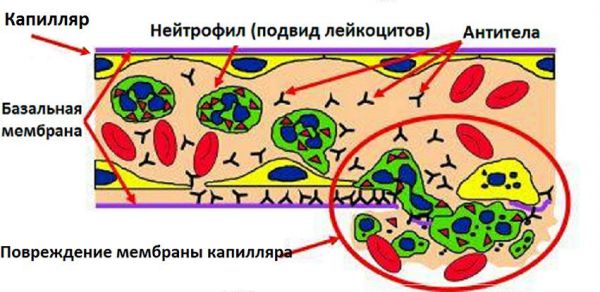
Эта заболевание является аутоиммунным. В крови появляются антитела, направленные против клубочковой мембраны в почках. Они связываются с чувствительными рецепторами клеток мембраны и запускают цепь реакций, приводящих к повреждению тканей.
Базальная мембрана состоит из коллагена и, в свою очередь, является поддерживающей конструкцией для внутреннего и наружного эпителия сосудов, и они вездесущи в организме человека. Но только в альвеолах легких и в почечных клубочках клетки базальных мембран страдают клинически, поскольку содержат большее количество структур, которые распознает иммунная система.
Кроме того, поскольку через почки постоянно проходит весь объем крови, то клубочковые клетки более доступны для циркулирующих антител.
Причины
В нормальных условиях эндотелий является барьером для антител. Но когда происходит повышение проницаемости сосудов, то начинается их осаждение на базальной мембране. Поскольку организм человека – замкнутая система и все процессы взаимосвязаны, то факторы, вызывающие повреждения в легких, затем неминуемо причинят и повреждение почек. Таким образом, причиной увеличения капиллярной проницаемости могут стать:
- увеличение капиллярного гидростатического давления;
- высокие концентрации кислорода во вдыхаемом воздухе;
- вдыхание металлической пыли, лекарств, кокаина, табакокурения;
- бактериемия;
- наличие в крови эндоксинов;
- воздействие летучих углеводородов;
- инфекции различной природы.
Также многие клиницисты склоняются к версии о генетической природе заболевания. Люди с определенным типом антигенов лейкоцитов человека более восприимчивы к этому заболеванию и имеют худший прогноз на его течение.
Возможно, именно этим обусловлено то, что чаще всего синдром гудпасчера встречается у мужчин белой расы в возрасте от 20 до 30 лет, а затем у женщин в старшей возрастной группе – за 60 лет. Хотя, в общем, заболевание довольно редкое, ему подвержены 0,5-1,8 % человек на миллион в год.
Как проявляется
Первые симптомы синдрома гудпасчера могут быть довольно общего характера:
- усталость;
- тошнота и рвота;
- затрудненное дыхание;
- бледные кожные покровы.
Если первым болезнь поразила легкие, то может нарастать одышка, появиться постоянный кашель, кровохарканье.
Почечные проявления заболевания будут следующими:
- появление крови в моче;
- образование пены;
- отеки нижних конечностей;
- повышенное кровяное давление;
- болезненное и затрудненное мочеиспускание;
- боль в спине ниже ребер;
- нарастание отеков всего тела.
Наиболее серьезным последствием синдрома является почечная недостаточность, которая может потребовать диализа или пересадки почки.
Диагностика
Анализ мочи
При общем анализе мочи показатели характерны для повреждения почек при гломерулонефрите.
В моче обнаруживается белок. Это важный симптом заболевания. Протеинурия критически высокая в первые дни и может достигать до 5 г/сутки. Большую часть белка составляют альбумины и незначительное количество глобулины и фибриноген.
Микро- и макрогематурия. Появление крови в моче может быть в разном объеме. Макрогематурия дает заметный красноватый цвет «мясных помоев». Эритроциты проникают в мочу через поврежденные капилляры в клубочках или же являются частью гемаррагического экссудата.
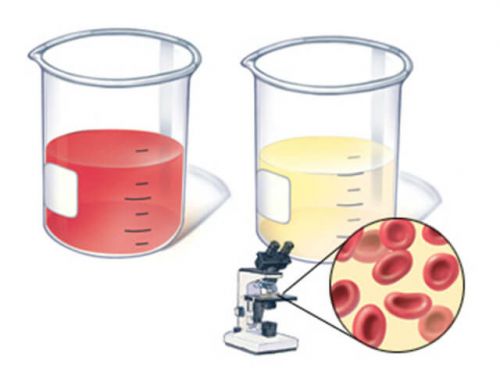
Макрогематурия при гломерулонефрите – кровь заметна в моче невооруженным глазом, микрогематурия – только при микроскопическом исследовании
Также могут быть найдены, но необязательно, клетки почечного эпителия, гиалиновые и эритроцитарные цилиндры.
Анализ крови
Общий анализ крови показывает повышение СОЭ, снижение содержания белка, анемию.
Биопсия
Это процедура чрезкожного забора пробы ткани почки для исследования с помощью микроскопа и иммунологических реакций. Проводиться под местным обезболиванием с визуальным контролем УЗИ или КТ. Поскольку метод получения материала для исследования инвазивный, то используется только в случае, когда по-другому подтвердить диагноз нет возможности.
При микроскопии можно обнаружить морфологически изменения, которые называются эпителиальные полулуния. Они находятся в капсуле Боумена, имеют серповидную форму. Это отличительный патологический знак.
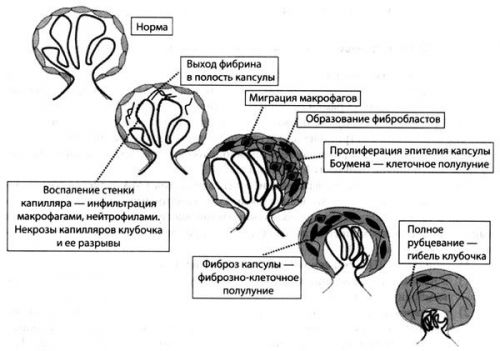
Нередко быстропрогрессирующий гломерулонефрит, к которому относят синдром гудпасчера также называют гломерулонефрит с полулуниями
Изначально полулуния состоят из макрофагов и разросшихся эпителиальных клеток клубочков. Затем они пропитываются фибриногеном и становятся плотными, фиброзными. Полулуния начинают сдавливать сосулы в клубочке, чем нарушают процесс фильтрации. В конечном итоге происходит их атрофия, что является предпосылкой для развития почечной недостаточности.
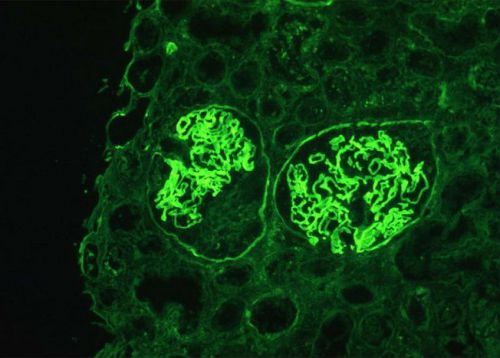
Иммунофлюоресцентная микроскопия. Видны гладко линейно окрашенные клубочковые базальные мембраны с антителом к IgG. . На клубочке, расположенном левее также видно полулуние
Также заболевание характеризуется линейным отложением иммуноглобулинов группы G на базальной мембране клубочков, что может быть определено иммунофлюоресцентным методом. Именно это метод является золотым стандартом в дифференциальной диагностике синдрома гудпасчера, поскольку позволяет точно отделить его от простого обострения хронического гломерулонефрита.
Рентгенологическое обследование
При легочных проявлениях анти-БМК болезни, те есть наличия прожилок крови в мокроте или кровотечения, что называется «полным ртом», проводят рентгенологическое обследование. Картина может быть представлена как поодинокими облачными инфильтратами в легких, так и обильным кровоизлияниями. Легочное кровотечение обычно опережает почечные проявления на недели или месяцы.
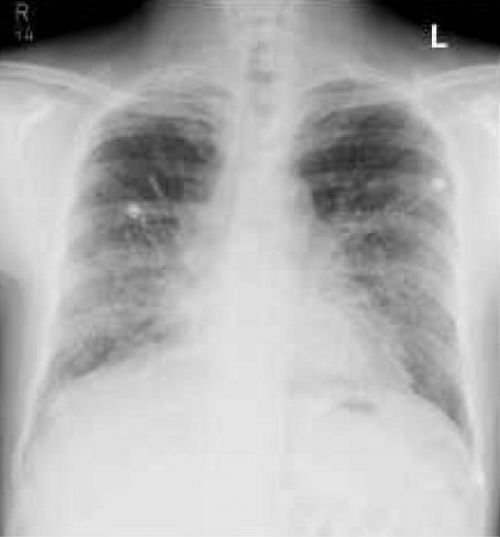
Двусторонние альвеолярные помутнения у пациента с альвеолярным кровоизлиянием из-за синдрома Гудпасчера
Лечение
Синдром гудпасчера требует быстрого и агрессивного лечения, которое направлено на:
- борьбу с антителами;
- контроль накопления жидкости;
- контроль высокого артериального давления;
- предотвращение повреждения легких и почек.
Тяжесть состояния пациента заставляет врачей прибегать к так называемой пульс – терапии. В первые дни лечения назначают сверхвысокие дозы препаратов.
Метилпреднизолон – 15 мг на кг веса/сутки – 3 дня, затем переводят на преднизолон в таблетках 1мг на кг веса/сутки.
Циклофосфамид – от 2 до 3 мг на кг веса/сутки с обязательным контролем над количеством лейкоцитов.
Азатриоприн – до 2 мг на кг веса/сутки, обычно назначают в случае непереносимости циклофосфамида.
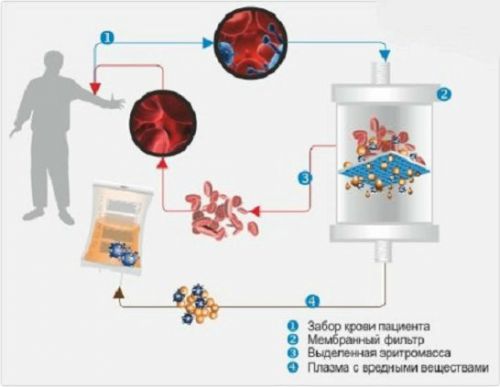
Применяют плазмаферез – аппаратную очистку крови от циркулирующих в ней антител. Во время этой процедуры из крови с помощью центрифуги отделяются красные и белые кровяные клетки, смешивают их с плазмозаменителем и возвращают назад в тело пациента. А компонент, ответственный за развитие заболевания, отфильтровывается и удаляется из крови.
Некоторым пациентам проводят искусственную вентиляцию легких или периодически подают кислород. Другим может требоваться переливание крови.
В случае, когда пациенту уже требуется диализная терапия, то функциональность почек едва ли может быть восстановлена.
Если поражение почек уже развилось в хроническую почечную недостаточность, то в ее терминальной стадии единственное решение это трансплантация органа.
Плазмаферез проводят периодически, в течение нескольких недель, а иммуносупрессивная терапия может длиться от полгода до 12 месяцев в зависимости от ответа на терапию.
Питание и диета
При синдроме гудпасчера питание или диета не играют роли в возникновении заболевания и не имеют профилактического воздействия.
На заметку
Синдром гудпасчера является легочно-почечным синдромом, который представляет собой группу острых заболеваний, и имеет следующие признаки:
- наличие гломерулонефрита;
- наличие антител-БМК;
- кровотечение в легких.
Заболевание является фатальным, если диагноз не установлен быстро и не назначено адекватное лечение.
Кровохарканье, как непарадоксально – благоприятный признак, поскольку позволяет раньше обратить внимание на заболевание и начать лечение.
Терапия чаще успешна, если начинать лечить до развития почечной и легочной недостаточности. В последние годы, на фоне агрессивной терапии кортикостероидами и иммуносупрессорами, выживаемость составляет 80% в пятилетнем периоде.


 Антифосфолипидный синдром и его симптомы
Антифосфолипидный синдром и его симптомы